5월 혁신의료기기 지원법 제정… 산업육성·제품개발 지원 초석 마련
기계학습 기술 기반 의료기기 공통 용어 개발·가이드라인 제정 계획
AI 의료기기 36건 허가 · 임상 시험 37건 승인… 매년 가파른 증가세
기계학습 기술 기반 의료기기 공통 용어 개발·가이드라인 제정 계획
AI 의료기기 36건 허가 · 임상 시험 37건 승인… 매년 가파른 증가세
식품의약품안전처가 국제의료기기규제당국자포럼(IMDRF) 'AI(인공지능) 의료기기 국제규제 실무그룹'(Artificial Intelligence Medical Devices, AIMDs)의 초대 의장으로 선출되면서, IMDRF와 우리나라 AI의료기기 현황에 대한 관심이 커지고 있다.
AI 의료기기는 컴퓨터를 이용해 기계학습 등으로 인간의 지적능력 일부 또는 전체를 구현하는 기술이 적용된 의료기기를 뜻한다.
6일 의료기기 업계에 따르면, 식약처는 지난달 25일 열린 IMDRF 운영위원회에서 회원국 만장일치로 AIMDs의 초대 의장으로 선출됐다. IMDRF는 의료기기 국제 규제조화를 주도하는 미국, 유럽 등 10개국 규제당국자 협의체로, 국내에서는 지난 2017년 12월에 가입했다.
IMDRF 실무그룹으로는 '국제 공통허가 심사서류'(주도국 캐나다), '개인맞춤형 의료기기'(호주), '체외진단 의료기기 분류 원칙'(러시아), '우수심사기준'(미국, 싱가포르), '이상사례용어'(일본), '의료기기 사이버보안'(미국, 캐나다) 등이 있다. 또한 '의료기기임상평가'(중국), '인공지능 의료기기'(한국)도 실무그룹으로 가동 중이다.
이 외에 '기준규격'(미국), '의료용 소프트웨어'(미국), '규제당국간 이상사례 보고체계'(유럽연합), '품질시스템 단일심사 프로그램'(캐나다), '환자정보등록시스템'(미국), '의료기기 고유식별코드'(유럽연합) 등이 가동됐다 종료됐다.
국제 공통허가 심사서류 실무그룹은 허가를 받기 위해 규제 당국에 제출하는 서류의 공통적인 템플릿(Template, 전자양식 포함)마련을 위한 가이드라인을 개발한다.
또한 개인맞춤형 의료기기 실무그룹은 개별 환자를 대상으로 하는 의료기기의 규제를 고려하기 위한 정의 및 규제절차 가이드라인을 개발하며, 체외진단 의료기기 분류 실무그룹은 GHTF의 동일명 문서를 현행화하기 위한 업데이트 작업을 계획 중이다. GHTF(Global Harmonization Task Force)는 IMDRF의 전신이다.
우수심사기준 실무그룹은 의료기기 허가 및 GMP 심사자 등 규제 심사자의 자격과 교육, 역량관리 요구사항을 수립하기 위한 가이드라인 개발과 단일 허가심사 체계를 목표로 허가 심사 업무를 수행하는 기관에 대한 요건 을 마련 중이다.
또한 이상사례용어 실무그룹에서는 IMDRF 의료기기 이상사례용어 및 코드 개발 및 조화를 위한 가이드라인을 개발하며, 의료기기 사이버보안 실무그룹에서는 의료기기 사이버보안에 대한 규제당국 간 모범사례를 공유하고 이에 대한 국제 공통 사전·사후 규제를 마련한다. 중국이 주도 중인 의료기기 임상평가 실무그룹은 규제당국 간 임상평가의 규제조화를 위한 GHTF 가이드라인을 업데이트한다.
AI 의료기기 실무그룹은 우리나라가 주도하는 신설 그룹으로, 의료기기에 적용되는 AI 기계학습 기술을 다루고 기계학습 기술 기반의 의료기기의 주요 공통 용어도 개발한다. 식약처는 AI 의료기기의 정의·적용대상 등 각종 국제 가이드라인을 제정할 계획이다.
한편, 식약처는 그동안 AI 의료기기 개발을 지원하고 선도적인 규제환경을 조성하기 위해 다양한 노력을 기울여 왔다. 2017년 세계 최초로 '인공지능 의료기기 허가·심사 가이드라인'을 마련하는 등 총 6개의 가이드라인을 발간해 국내에서 15개사 36개의 AI 의료기기를 허가할 수 있는 밑거름이 됐다.
또한, 지난 5월 시행된 '의료기기산업 육성 및 혁신의료기기 지원법'을 제정해 AI 의료기기 등 혁신의료기기 산업 육성 및 제품개발 지원을 위한 초석을 마련했다.
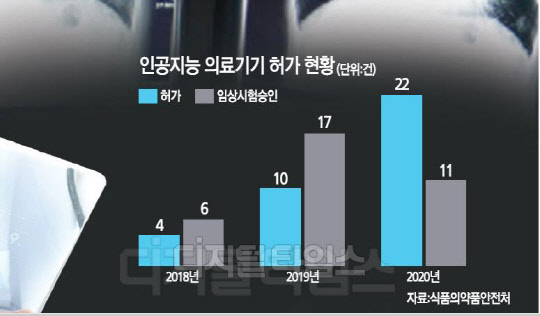
식약처는 현재까지 총 36건의 AI 의료기기를 허가했고, 총 37건의 임상시험을 승인했다. 허가 건수는 2018년 4건에서 지난해 10건으로 늘었고, 올해 들어서는 22건을 허가(6월26일 기준)했다. 골연령을 분석하는 AI 의료기기인 뷰노의 '메드- 본 에이지', 크레스콤의 'MediAI-BA', 헬스허브의 'Boneage.io', 레이언스의 'Xmaru Pro BoneAge', 'Xmaru Pro CXR' 등이 대표적이다. 폐결절 검출·유방암 진단·흉부 이상부위 검출 등을 보조하는 루닛의 '인사이트'도 있다. 임상시험 승인 건수는 2017년 3건에서 2018년 6건, 2019년 17건으로 늘었고, 올해는 6월26일 기준 11건의 임상시험을 승인했다.
김수연기자 newsnews@dt.co.kr
[ 저작권자 ⓒ디지털타임스, 무단 전재 및 재배포 금지 ]